 发病机制
发病机制
发病机制:
1.类风湿关节炎发病机制的认识过程 类风湿关节炎发病机制的研究是一个漫长的过程,至今也没有得到明确的定论。回顾这一认识过程,可以更清楚地认识类风湿关节炎。
早在20世纪20年代,就有人提出感染可以导致RA,并且将RA作为感染性疾病进行治疗,尽管有一定的疗效,但是一直没有找到感染的致病微生物。在20世纪40年代,Waaler、Rose及其同事发现了类风湿因子,并将它与RA的出现联系在一起,以后陆续发现了B细胞、免疫复合物、补体等在RA发病中的作用。体液免疫的异常,被认为是RA发病中起关键作用的因素。这种思想统治了近40年。直至20世纪80年代,随着对细胞因子的认识逐渐深入,提出RA是由T细胞介导的自身免疫性疾病,在此基础上发展出许多针对T细胞的治疗方法,并取得了一定的疗效。但是与此同时,又发现了一些不支持T细胞在RA发病起主要作用的证据。20世纪后期,随着对RA滑膜细胞的认识逐渐深入,发现成纤维样滑膜细胞具有转化的特性,由此逐渐将固有免疫的作用提到了重要的位置。
对RA发病机制的认识过程,实际上也是对RA整个疾病的认识过程。随着生物技术的提高,研究手段的不断丰富,在21世纪,RA的发病机制必将取得突破性的成果。
2.滑膜组织的异常增生
(1)滑膜组织的结构:滑膜层位于关节囊的内层,分为滑膜内层和滑膜下层。滑膜内层,又称滑膜衬里层,是由疏松排列的细胞组成,它介于滑膜与滑液之间。该层有两种主要的细胞类型:巨噬样细胞(又称A型滑膜细胞)和成纤维样细胞(又称B型滑膜细胞)(表3)。
前者是由骨髓分化而来,表达巨噬细胞表面标记物,并高度表达HLA-DR;而后者缺乏特异的HLA-DR分子标记。在生理条件下这两种类型细胞的数量,前者占20%~30%,后者占70%~80%。滑膜内层的细胞之间缺乏紧密连接,而且与滑膜下层的细胞间没有基底膜相隔,这也为RA滑膜细胞的大量增生提供了结构基础。滑膜下层,又称滑膜衬里下层,主要由成纤维细胞、脂肪细胞、巨噬细胞、肥大细胞、胶原纤维和蛋白多糖组成,该层含有丰富的血管和淋巴管,主要对滑膜细胞起营养作用。
(2)类风湿关节炎滑膜组织的变化:正常人的关节滑膜内层仅1~2层细胞组成,而RA患者的滑膜内层通常有4~10层细胞(有时甚至超过20层)。这些细胞不仅在数量上异常增多,而且在功能上处于异常活跃的状态,它们可以分泌大量的细胞因子、信号分子和蛋白酶,加速关节破坏的进程。另外,RA滑膜中还有大量的炎性细胞浸润,如T细胞、B细胞和单核细胞,以及微血管数量的显著增加。
(3)滑膜组织中的细胞因子:
①细胞因子在RA滑膜病变中起着核心作用。细胞因子系统通过作用于多种细胞并相互调节形成一个复杂的网络。在RA的滑膜中,不仅T淋巴细胞可以分泌多种细胞因子,如IL-2、IFN-γ、IL-4等,而且巨噬样滑膜细胞和成纤维样滑膜细胞也可分泌多种细胞因子,例如肿瘤坏死因子-α、IL-1、IL-12、IL-6、IL-15等。反之,这些细胞因子会刺激或抑制上述细胞进一步分泌细胞因子。
目前对RA细胞因子的研究发现,RA滑膜细胞产生的细胞因子呈稳定、持续的表达。体外试验表明,多种物质可刺激滑膜细胞产生细胞因子,而且,细胞因子本身也是产生细胞因子强有力的刺激因子。在T细胞的免疫应答下调后,滑膜中的巨噬细胞和滑膜成纤维细胞以旁分泌或自分泌方式产生的细胞因子使炎症反应得以延续。另外,在滑膜或滑液中可检测到多种细胞因子,它们不仅能够解释滑膜衬里层细胞增生的原因,而且能够诱导HLA-DR和黏附分子的表达,以及滑膜微血管的形成。
RA滑膜的炎症反应涉及的细胞因子种类非常多。研究表明肿瘤坏死因子-α和IL-1在RA的发病中起着极其关键的作用。这两种细胞因子刺激滑膜成纤维细胞增生,分泌IL-6、GM-GSF、趋化因子以及基质蛋白酶和前列腺素等效应分子。其中,GM-CSF是由滑膜巨噬样细胞和成纤维细胞共同分泌的,它不但可以诱导IL-1的分泌并形成一个正反馈环,而且还可与肿瘤坏死因子-α共同作用于巨噬细胞增加HLA-DR的表达。另外,由巨噬细胞和成纤维细胞分泌的细胞因子还可以间接作用于局部T细胞和B细胞的活化,其中包括RF的产生。
肿瘤坏死因子-α主要由滑膜衬里层的滑膜巨噬细胞产生。已证实肿瘤坏死因子-α作用的靶目标是某些抗肿瘤坏死因子-α成分(如可溶性肿瘤坏死因子-α受体等)。影响肿瘤坏死因子-α产生的因素包括免疫复合物、补体的活化、细胞外基质成分和局部细胞因子的表达。这里特别要提到局部细胞因子的表达。近来的研究表明,由滑膜细胞分泌的IL-15不仅可以促使T细胞的移位、活化以及趋化因子的产生,还能增加肿瘤坏死因子-α的产生。研究显示,不仅在RA滑膜内检测到了IL-15的mRNA和蛋白,而且,在体外实验观察到可溶性IL-15受体可以直接减少滑膜巨噬细胞产生肿瘤坏死因子-α,或者通过与IL-1、IL-6以及肿瘤坏死因子-α共同促进T细胞/巨噬细胞间的相互作用。
②研究表明,肿瘤坏死因子-α被认为是滑膜炎症反应的关键性细胞因子,可能的证据是:
A.肿瘤坏死因子-α的生物活性直接或间接参与RA多种病理过程,包括炎性细胞的聚集和激活、滑膜细胞的增殖、诱导成纤维滑膜细胞产生骨和软骨破坏的细胞因子和蛋白酶、刺激巨噬细胞产生其他细胞因子等(图2)。
B.在RA滑膜组织中肿瘤坏死因子-α和肿瘤坏死因子-α受体明显升高。
C.在体外,抗肿瘤坏死因子-α抗体对IL-1及其他,前炎性细胞因子的产生有抑制作用。
D.过分表达肿瘤坏死因子-α的转基因小鼠产生侵蚀性关节炎,其组织学特点与RA类似。
E.关节炎的动物模型证实,抗肿瘤坏死因子-α物质可以减轻病变程度。
F.对RA予抗肿瘤坏死因子-α治疗可以产生较好的临床效果。最近的研究显示,虽然给予抗肿瘤坏死因子-α治疗可以有效地控制病情,但一旦停药疾病即复发,而且抗肿瘤坏死因子-α治疗并不是对所有的患者都有效。因此,有研究者观察到,RA持续存在的滑膜炎症并不是由产生肿瘤坏死因子-α的自分泌反馈环所造成的,还有其他重要因素的参与。因此,今后的研究需要进一步探讨肿瘤坏死因子-α在炎症细胞因子中是否具有独特的地位等问题。
IL-1也是滑膜炎症反应的关键性细胞因子。在RA滑膜中,它也是由滑膜巨噬细胞产生的。多种因素可以诱导IL-1的产生,例如,免疫球蛋白的Fc段、免疫复合物、胶原片段以及T细胞的信号分子等。在滑膜中,IL-1可以诱导成纤维细胞的增生,刺激滑膜细胞合成IL-6和GM-CSF,并可增加成纤维细胞产生胶原酶。另外,它还可以刺激滑膜细胞增加与细胞相连的或细胞外的纤溶酶原激活剂的活性。现已证明,IL-1β是一种刺激骨骼吸收的破骨细胞的活化因子。IL-1还可刺激内皮细胞分泌黏附因子,包括VCAM-1和ICAM-1。RA的动物模型显示IL-1是调节骨与软骨破坏的重要的细胞因子。
③T淋巴细胞作为RA滑膜中数量最多的一类炎性细胞,而在滑液中,很少能检测到T淋巴细胞分泌的细胞因子,并且疾病的发生和发展并不会造成T细胞分泌的细胞因子发生变化。例如,无论在RA早期还是活动期IFN-γ在关节内表达的数量基本不变。为什么RA滑膜中T淋巴细胞分泌的细胞因子数量如此之少呢?可能有以下一些原因:
A.细胞活性受到局部抑制是造成T细胞免疫应答能力下降的原因之一。例如,在RA滑液中可检测到IL-1受体拮抗剂(IL-1Ra)和TGF-β这两种T细胞的抑制剂。另外,滑液中某些非特异性成分如hualuronate,也可以间接抑制T细胞的活性。在RA患者滑膜组织的微环境中,由巨噬细胞分泌的肿瘤坏死因子-α和由滑膜组织细胞分泌的IL-10均可下调T淋巴细胞的功能。
B.与T细胞受体(TCR)信号异常相关。特别是经p38有丝分裂原活化的蛋白激酶(MAPK)信号转导途径的刺激,滑液中T细胞可以减少酪氨酸的磷酸化。而且,TCRζ链的酪氨酸磷酸化也存在异常,研究发现TCRζ链的水平下降,这表明RA中有TCR装配异常。
C.与T细胞功能的抑制剂存在缺陷有关。体外实验观察到,RA中IFN-γ的产生明显受到抑制,但是,当加入吲哚美辛后这种情况可被纠正。有研究显示,T细胞产生IFN-γ的减少是因为RA细胞对PGE反应的敏感性增加。而且实验证明,来自RA病人外周血的T细胞产生IL-2减少,当加入吲哚美辛后上述这种情况也可得到部分改变,这也进一步说明RA病人对PGE有更高的敏感性。
D.可能是这些细胞因子在滑膜中以微量的形式就足以维持疾病病理变化的持续进行。不过,RA滑液中T细胞分泌的IFN-γ作用很重要。它是MHCⅡ类抗原最有效的诱导剂,可以激活单核巨噬细胞,还能诱导VCAM-1和ICAM-1等黏附因子在内皮细胞的表达,并且能够协助招募炎性细胞向损伤部位聚集。另外一个重要的作用就是IFN-γ可以改变细胞外基质的合成与降解之间的平衡。总之,目前对T细胞分泌的细胞因子其准确的功能还知之甚少。
④在RA滑膜炎症反应的过程中,滑膜内的细胞还释放各种具有抗炎症的细胞因子,例如IL-1受体的拮抗剂、可溶性肿瘤坏死因子-α p75和p55受体、可溶性IL-1受体、IL-16、IL-11、IL-13和IL-10等。在RA炎症反应的调节过程中,这些抗炎症细胞因子的表达也有所增加,但仍不足以抑制关节滑膜炎症的发生。研究发现,细胞表面脱落的可溶性肿瘤坏死因子受体p55和p75是在关节滑膜液中可检测到的两种受体,但其浓度不足以中和关节滑膜液中产生的内源性肿瘤坏死因子;与此相似,IL-1受体拮抗剂是IL-1的天然抑制剂,在许多RA患者滑膜液中表达的水平也较高,同样也不足以消除IL-1引起的炎性作用。目前的研究认为,促炎症性细胞因子和抗炎性细胞因子之间作用的失衡使细胞因子的内稳定遭到破坏,这是RA发病的重要特征。利用这些细胞因子无疑对RA的治疗很有价值。近年来,运用基因重组技术已研制出多种细胞因子的拮抗剂,并取得了令人满意的临床疗效。
(4)滑膜中信号分子的作用:通过各种刺激,细胞内信号转导系统将细胞表面已启动的细胞外信号转入核内,并在此整合转录因子的水平。转录因子结合特异的DNA位点,调节某些适当基因的表达。RA滑膜组织的异常增生与炎症反应相关,越来越多的证据表明有多种转录因子参与了这一过程。核因子κB(nuclear factor-κB,NF-κB)、激活因子蛋白-1(activator protein-1,AP-1)和分裂素激活的蛋白激酶(mitogen-activated protein kinase,MAPK)被认为在RA中起重要的作用。
(5)滑膜中细胞凋亡的作用:近几年,人们逐渐认识到细胞凋亡在RA发病中的作用。细胞凋亡是细胞程序性死亡的一种。细胞凋亡存在于正常生理情况下,是在个体发育、多细胞生物体的平衡和疾病发生中起重要作用的一种细胞死亡形式。滑膜细胞的大量增殖和炎症细胞的侵入是RA的典型特征。目前的研究认为这与细胞周期(增殖/凋亡)的失调有关。
近来的文献报道显示,利用DNA电泳、电子显微镜和TUNEL(DNAnick-end labeling)方法检测到滑膜组织中存在凋亡细胞。不过,这种凋亡细胞数量很少,这主要由于它们位于巨噬细胞周围,一旦出现很快就被巨噬细胞所清除。目前识别出3种与细胞表面相关的受体,它们是Fas抗原(CD95)以及两种肿瘤坏死因子受体,后者分别是55kD的肿瘤坏死因子-RⅠ和75kD的肿瘤坏死因子-RⅡ,其中Fas抗原是一种45kD细胞表面蛋白,许多类型的细胞表达此种膜细胞死亡受体。它们都属于肿瘤坏死因子/神经生长因子受体家族,参与调节细胞的生存和死亡。Fas配体(Fas-ligand,Fas-L)是40kDⅡ型转膜蛋白质,主要表达于活化的T细胞表面。它可诱导诸如B和T淋巴细胞、巨噬细胞或嗜中性粒细胞等易感靶细胞的凋亡。
RA滑液中活化的T细胞表面表达大量的Fas分子。Fas与Fas-L的相互作用,能够启动细胞凋亡。当IL-1β和肿瘤坏死因子-α占据各自细胞表面的受体时,它们也可通过这种机制引发细胞的死亡。研究发现,RA滑膜组织既含有Fas 的滑膜细胞和单核细胞,也含有表达Fas-L的活性T细胞和自然杀伤细胞。因此,在RA滑膜中,通过Fas/Fas-L的相互作用激活受体介导的滑膜细胞凋亡,这在细胞凋亡中起关键性作用。表达Fas-L的T细胞或自然杀伤细胞与滑膜细胞和单核细胞表面的受体Fas相互作用,也许在RA细胞增殖的自然缓解期起一定作用。反之,在RA细胞增殖阶段,Fas/Fas-L的相互作用有可能受到其他因素的影响或破坏。细胞内的蛋白Bcl-2家族有抑制或增强细胞凋亡的作用。CD4 CD28-T细胞Bcl-2的表达增加可使细胞凋亡受到抑制,因此造成滑膜组织中自身反应性细胞的克隆增殖。
试验表明,不仅RA的滑膜细胞表达Fas分子,而且骨关节炎的滑膜细胞表面也表达Fas。但是,抗Fas抗体可以诱导RA滑膜细胞出现凋亡,而无法诱导OA出现凋亡。而且Fas刺激某些细胞可以出现增殖,而不是凋亡。这说明Fas还可以通过其他因素调节滑膜细胞的增殖或凋亡。这些因素包括细胞内信号转导途径和抗凋亡因子。近来的研究表明,NF-κB、AP-1、MAP激酶等信号转导途径参与了这一过程。有文献认为,理解RA滑膜细胞中Fas和肿瘤坏死因子-α介导的信号途径非常重要,这些因子能激活其信号分子如转录因子NF-κB,由此诱导凋亡抑制基因Bcl-xL和Survivin的表达,刺激滑膜细胞的增殖,并抑制成纤维细胞的凋亡。有研究表明,Fas无法激活NF-κB,但可以介导由JNK(属于MAP激酶)/AP-1诱导的凋亡;由肿瘤坏死因子-α激活的NF-κB在滑膜细胞增殖的调节中起着重要的作用。因此认为,NF-κB的调节作用在滑膜细胞的增殖或诱导其凋亡等方面都有很重要的作用。
还有一种因素对细胞凋亡产生影响,即肿瘤抑制基因p53。另外,它还是细胞周期、DNA复制、细胞分化和DNA修复等重要的调节剂。虽然p53本身不是原癌基因,但是它在c-myc等原癌基因的转录调控下,为诱导细胞周期停滞和细胞凋亡提供了重要的信号。在氧化应激的作用下,活性氧和活性氮的产生增加,造成DNA的损伤,使p53水平升高。功能性p53可以诱导细胞周期停滞、DNA修复或细胞凋亡。但是突变的p53可持续造成DNA的损伤,出现细胞转化而不出现细胞凋亡。研究发现,在RA的滑膜衬里层和衬里下层发现突变的p53,而且它的表达明显升高。故认为,p53对RA滑膜细胞的增殖也有一定的作用。
总之,在RA存在很多抑制细胞凋亡的因素,这也是引发滑膜细胞增殖和炎症细胞侵入的重要因素。
(6)新生的微血管:目前已认识到新生的微血管在炎症反应过程中起着极为积极的作用。它不仅可以作为机体选择细胞进入炎症组织的一种手段,而且还是促进组织生长和补充组织营养的决定因素。
在RA滑膜组织中可以看到大量新生的微血管,类似于肿瘤组织和创口愈合组织中所看到的。在多年以前就已有研究者发现了这一现象,并指出新生的微血管在滑膜炎症发展过程中的重要性。此后在胶原性关节炎的动物模型中证实了这一结论。而且研究表明,如果阻断炎症过程中血管的形成,那么可以缓解RA的病情发展。因此,RA中新生的微血管是炎症发生和发展过程中的基本条件,因为这些血管不仅可以用以招募炎性细胞,还可为增殖的滑膜组织提供营养物质。
RA滑膜的新生微血管数量明显增加,主要为毛细血管极高柱状内皮的毛细血管后微静脉。后者常位于淋巴滤泡中心。细胞间连接松弛和基底膜的不完整状态造成新生血管的通透性升高,为参与炎症反应的成分持续进入病变组织提供了结构基础,有利于维持并促进炎症反应的进行。
滑膜炎表现为大量的滑膜组织增殖,虽然伴有新生的血管形成,但从滑膜组织单位面积的分配上,这种新生血管的数量远远不能满足滑膜的需要。而且,研究显示RA滑膜的耗氧量是正常的20倍。这种局势必然造成局部滑膜组织出现缺血缺氧。另外,随着炎症的发展,关节腔内滑液逐渐增多,腔内压力也随之升高,都可造成血流减慢,滑膜组织缺氧。
滑膜组织的低氧状态是血管形成有效的刺激因素。新生血管形成的机制之一就是产生诸如血管内皮生长因子(vascular endothelial growth factor,VEGF)等血管形成因子。VEGF能增强局部血管的通透性,刺激内皮细胞进行有丝分裂,是一种特异性的促内皮细胞分裂因子,同时伴有某些趋化的特性。不仅在RA病变关节的积液中可以检测到高浓度的VEGF,而且在滑膜组织的血管内及其周围也可检测到。另外,VEGF的受体也存在于上述同一区域内。VEGF在滑膜衬里层呈高表达,培养的成纤维样滑膜细胞暴露于低氧环境和有IL-1存在的条件下,也可以产生VEGF。
除了低氧状态能够刺激RA滑膜新生微血管形成外,包括IL-8、成纤维细胞生长因子(fibroblast growth factor,FGF)和肿瘤坏死因子-α等在内的炎性细胞因子均被证明能刺激和参与血管新生过程。其他一些血管形成因子包括可溶性E-选择素和可溶性VCAM,也刺激新生血管的形成。
3.自身免疫的异常
(1)T细胞在类风湿关节炎中的作用:
有关T细胞在RA发病机制作用的假说:几十年来,围绕T细胞在RA发病机制的作用提出过多种假说。最初被多数研究者认同的,即认为RA是在遗传和环境因素的作用下由T淋巴细胞介导的自身免疫性疾病,因为有很多证据表明T细胞在RA发病中起着重要的作用:
①RA滑膜组织中浸润的细胞以单核细胞为主,其中30%~50%是T淋巴细胞。
②这些T细胞的绝大部分表达活化标记分子。
③针对T细胞的免疫治疗对RA有一定的疗效,这种疗法主要能够部分消除或抑制T细胞的活性。例如,用全身淋巴放疗或环孢素A治疗可以使病情得到缓解。
④在胶原性关节炎和佐剂性关节炎等动物关节炎模型中,自身反应性T细胞可以使患病动物出现疾病的转移。不过,还有一些重要的问题尚未解决,包括:
A.滑膜T淋巴细胞是否是病程进展的诱发因子。
B.T细胞浸润滑膜是否是关节内炎症反应的结果。
C.参与T细胞活化的自身抗原尚未找到。
近几年又提出一种新的假说,即在疾病发展过程中,存在外周免疫耐受机制的异常、淋巴细胞的异常增殖和T细胞内环境稳态的失衡。研究资料显示,在RA中,T细胞免疫的失调不仅仅局限于炎症反应的部位,更确切地说,在T细胞免疫耐受出现缺陷的基础上,滑膜形成具有慢性破坏性的淋巴组织。对动物模型的研究提示,这些自身反应性T细胞的增殖源自调控淋巴细胞增殖和T细胞内环境稳态的机制出现异常。
(2)RA滑膜中T细胞的特点:RA滑膜中的CD4 T细胞有以下一些重要的特点:
①表达CD45RO的同工型,使它们具有记忆细胞的特点,表明曾与抗原接触过。滑膜中naive T细胞数量非常少。在这个方面,滑膜与诸如淋巴结等周围淋巴组织不同。
②滑膜CD4 T细胞表达CD69,后者是一种早期活化的标志分子。RA患者的外周血T细胞很少表达这类分子。据文献报道,滑膜T细胞表达的CD69与疾病的严重程度相关,这也提示CD69 T细胞在疾病中的作用。
③现已明确,只有在两种信号的参与下抗原刺激的T细胞才能获得最大的活性,这两种信号分别是TCR-肽-MHCⅡ复合物和共刺激分子(co-stimulatory molecule),后者包括T细胞表面表达的CD28和CTLA-4以及APC表面表达的B7-1(CD80)和B7-2(CD86)。RA滑膜内的T细胞也表达CD28和CTLA-4,而且在关节内的APC也可见其配体B7。CD80和CD86与CD28或CT-LA-4结合,主要参与辅助刺激T细胞的活化,引起T细胞的增殖以及IL-2的分泌。不过,在RA血液和关节内检测到CD28-T细胞,这些细胞可与自身抗原产生应答,而且可以逃脱外周的免疫耐受。近来的研究表明,CTLA-4随着T细胞的活化出现上调,可以传递抑制信号而下调T细胞的增殖。CD40是另一种共刺激分子,表达于多种类型细胞的表面,包括B细胞、单核细胞/巨噬细胞、内皮细胞和成纤维样滑膜细胞。CD40的配体被称为gp39、CD40L或CD154,位于有活性的T细胞表面。在RA滑膜中可检测到CD40及其配体CD40L。特别是在IFN-γ存在的情况下,CD40与其配体之间的反应可以辅助刺激T细胞的活化、上调黏附分子、产生细胞因子和趋化因子、同型免疫球蛋白的转型以及产生一氧化氮。CD40的配体还可以诱导单核细胞的活化和树突状细胞的分化,以上这些都会影响RA的发展。如果缺少这些共刺激分子,T细胞将不会被激活,则会导致抗原识别的免疫耐受(tolerance)。
④聚集于滑膜的记忆性T细胞在功能上有一定的缺陷。滑膜T细胞表达的表型提示细胞凋亡存在异常(呈低Bcl-2和高Bax和Fas配体的表达),而且,滑膜T细胞的死亡率很低。相反,如果将这些滑膜中的T细胞分离出来,其生存率并不高。因此说明滑膜可以通过某些特殊的功能抑制细胞凋亡和促进细胞存活(表4)。
(3)RA中T细胞的作用:目前认为,T细胞在疾病的早期起着非常重要的作用。下面的这一假设可以解释T细胞是如何在RA中起作用的。首先,naive T细胞离开胸腺后,在外周循环中被激活,它们的表面表达活化标记物,并逐渐增强与内皮细胞黏附的能力,随后进入病变的关节内。如果没有持续的抗原作为刺激,T细胞表面表达的IL-2受体将逐步减少,一部分T细胞转变为记忆性T细胞。当关节内一小部分的记忆性T细胞识别出表达于抗原递呈细胞(APC)表面与MHC分子结合的抗原肽之后,T细胞被激活。其中滑膜细胞、巨噬细胞、树突状细胞和B细胞等APC表面都可携带MHCⅡ类分子,而MHCⅡ类分子可以与某种抗原肽相结合,并通过APC递呈给T细胞,与T细胞表面的TCR结合。这些浸润于滑膜组织的T淋巴细胞,通过与抗原递呈细胞上的“未知抗原”相结合,激起一系列免疫炎症反应,并分泌IFN-γ、IL-17、IL-2等多种细胞因子。
如前所述,根据光学显微镜和免疫组化的研究显示,浸润于RA滑膜组织的T细胞主要为CD4 记忆性T细胞(CD45RO )。CD4 T辅助细胞又可根据它们分泌细胞因子的种类分为两个亚型,即Th1和Th2。前者可产生包括IFN-γ、IL-2和IL-17等在内的促炎症性细胞因子,主要介导迟发型超敏反应,后者则可产生包括IL-4、IL-5、IL-10和TGF-β等在内的抗炎性细胞因子,主要参与变态反应以及抗体的活化和转型。在滑液中,很少能检测到T淋巴细胞分泌的细胞因子。近几年,有研究者利用RT-PCR或原位杂交技术发现,RA滑膜中以Th1细胞因子为主,而Th2细胞因子的水平极低。现尚不清楚T细胞分泌的细胞因子在RA发病中的作用。不过,近来的研究发现,滑膜T淋巴细胞分泌的IL-17是一种重要的细胞因子,尽管它的含量很低。它与IL-1和肿瘤坏死因子-α的许多作用相似,可以增强成纤维滑膜细胞产生胶原酶和其他细胞因子。更重要的是,RA滑膜组织中的IL-17可以协同IL-1和肿瘤坏死因子α激活滑膜细胞,增强局部的炎症反应。
正如前面所述,浸润滑膜的T细胞产生的细胞因子在滑液中的含量很低,那么,T细胞是如何来激活巨噬细胞的呢?滑膜内的各种细胞主要通过细胞因子的作用产生相互作用,也可以通过细胞直接接触的方式产生作用。最新的研究结果显示,患者滑膜组织中巨噬细胞的活化主要可能源自于巨噬细胞和T淋巴细胞之间的直接接触。CD4 T细胞浸润滑膜组织后直接和巨噬细胞接触,引起巨噬细胞的活化。活化的巨噬细胞分泌产生肿瘤坏死因子-α和IL-1等促炎症性细胞因子,同时也分泌产生IL-15,后者可促进由T细胞和巨噬细胞之间接触引起的巨噬细胞活化,而且它还能刺激T细胞,致使更多的T细胞得以活化。随着巨噬细胞的进一步活化,还会产生更多的肿瘤坏死因子-α和IL-1。近来的研究表明,T细胞与成纤维样滑膜细胞之间也存在细胞的直接接触,引起成纤维样滑膜细胞的进一步活化,分泌细胞因子和蛋白酶。值得注意的是,T细胞与滑膜细胞的直接接触并不需要活化的T淋巴细胞参与,说明这种反应可以通过非抗原依赖的方式完成。
近几年研究发现,RA滑膜组织形成具有淋巴结某些特征的异位淋巴组织,T细胞在这一形成过程中起着极其重要的作用。许多资料表明,淋巴样器官形成可以发生在诸如滑膜等淋巴外组织中。浸润于滑膜组织的淋巴细胞形成的滤泡样结构主要由CD4 T细胞和B细胞以及滤泡间的CD8 T细胞组成。在一些RA患者的滑膜滤泡样结构中发现有生发中心形成,说明关节中存在淋巴结样结构。生发中心的形成需要抗原特异性T细胞和B细胞之间的相互作用,以及通过共刺激分子表达的,且与T细胞和B细胞表面抗原特异性受体紧密相关的信号。现已证明这种生发中心的形成(一种介导抗原的收集和获得性免疫应答的复杂淋巴微型结构)是赖T细胞的,因为有证据表明,位于滑膜滤泡样结构中的B细胞产生的抗体有明显亲和性成熟的表现。推测滑膜组织中这种淋巴样器官的形成可能是免疫应答的结果(表5)。
总之,滑膜中活化的T细胞可以通过产生或诱导某些介质,调节巨噬细胞、滑膜细胞和B细胞的功能,加重RA滑膜的炎症。
(4)RA滑膜中T细胞的克隆增殖:关于RA滑膜T细胞是由少数几个T细胞克隆增殖而来,还是由多克隆激活的结果这一问题,目前还有争论。T细胞经活化后可出现克隆增殖。因为滑膜中T细胞的活化导致T细胞受体(TCR)成分的改变,故研究TCR成分可以更好地理解T细胞活化的性质。不过有关对滑液和滑膜组织中TCR Vα和Vβ基因片段出现的频率的研究得到矛盾的结论,这是由于研究该问题的方法不同而造成的。有的结论认为,如果超抗原参与了T细胞的活化或由于某种抗原特异性反应导致一组相关的T细胞增殖,那么增殖的T细胞有可能分享同一特殊的Vβ成分。但是,也有人持不同的意见,即RA T细胞源自许多不相关的克隆。因为大多数的研究表明TCR的成分确实有所改变,但这些改变并不明显,而且并不是所有的研究中都发现了这种改变。多项研究显示TCR Vα和Vβ的成分存在多样性。滑膜组织T细胞的分析表明,某些T细胞呈克隆增殖,但是,根据TCR的结构,这些T细胞的成分又是不同的。对这些观察最为合理的解释是,滑膜组织中只有一小部分T细胞的增殖是源自对抗原的免疫应答。增殖的T细胞表现出多样性,这也说明病变部位识别的抗原谱很广。
目前关于T细胞克隆增殖主要有两种结论,它们是:①T细胞的克隆局限于关节内,表现为对局部抗原的反应;②T细胞的克隆,呈非限制性分布方式,说明在保持T细胞多样性方面存在普遍缺陷。因此说,T细胞克隆增殖的反应可能是多种多样的,并不仅仅针对一个(或一些)引发疾病的T细胞克隆,这也可能是造成疾病异质性的原因。
(5)B细胞在类风湿关节炎中的作用:
①RA中的B细胞:RA中T细胞和B细胞的作用尚未全部被了解。很多研究者将自身免疫性疾病的研究重点放在T细胞的作用上。由于目前尚无确凿的证据显示RA中的自身抗体直接参与组织的损害,从而忽视了抗原一抗体复合物在疾病中的重要作用。大多数RA患者都可检测到自身抗体,而且有60%~80%的病人存在高亲和力的自身抗体。例如,类风湿因子就是对自身IgG恒定区产生的自身抗体。从对RF的研究发现,关节中形成的免疫复合物以及该免疫复合物对补体系统的激活,都可造成关节的破坏。B细胞除了产生抗体外,活化的B细胞还可识别抗原,而且它向T细胞递呈抗原的能力优于巨噬细胞,所以B细胞还是一类重要的抗原递呈细胞。
②正常的滑膜组织是无细胞结构的,而RA的滑膜中可以看到大量单核细胞的浸润。除了巨噬细胞,30%RA患者的滑膜发现了由T细胞和B细胞形成的滤泡样结构,其中有的形成生发中心(germinal centre),说明关节中存在淋巴组织样结构。细胞因子对这种异位淋巴组织的形成起着关键的作用。生发中心是抗原激活的B细胞发展成为记忆性B细胞和浆细胞的微环境,也是体液免疫反应发生亲和性成熟的部位。与从人扁桃体分离出的生发中心细胞一样,滑膜组织生发中心的B细胞表达低水平的CD38,并能够下调免疫球蛋白受体。在生发中心活化的B细胞依赖T细胞的形式诱发克隆增殖。研究显示,通过显微解剖从RA患者冰冻的滑膜组织中可以直接分离得到增殖的B细胞。
③活化的B细胞既可存在于外周血中,也可出现于滑膜组织中。细胞因子在抗体的产生和转型中起着非常重要的作用。IL-2在诱导所有同型免疫球蛋白中起主导作用。因为在缺少IL-2的情况下,没有其他细胞能够影响淋巴细胞的活化、增殖或分化。IL-4对B细胞有促进生长的作用,并可诱导MHCⅡ类抗原在B细胞表面的表达。
④目前已提出不少有关IgG何以具有免疫原性的假说。
A.当Ig分子聚集形成聚合物后或IgG与特异性非IgG抗原形成复合物,有可能暴露出新的IgG抗原决定簇。
B.RA患者IgG结构的异常可使IgG产生免疫性。例如,IgG铰链区的缺陷可能增加与B细胞膜上Fc受体结合的亲和力。另外,T细胞抑制剂的缺失可使得B细胞产生抗IgG的抗原决定簇抗体。
C.IgG自身抗原的活性与IgG糖基化结构的改变相关。例如,半乳糖基转移酶活性的异常可能会增加RA发生的危险性。
自身或非自身抗原产生的免疫应答是RA产生或持续存在的原因这一假设得到许多研究者的支持。作为体液免疫反应的效应细胞,B细胞在RA的发病中起着重要的作用。
⑤临床观察到的一些现象与抗原作为RA的病因这一结论相符:
A.一小部分RA患者在经历了几个月的活动期后会进入一段相当长的临床缓解期,这提示患者可能接触过某种抗原,但这种抗原随后被清除。
B.随着多关节病变的进展,约20%RA患者出现某一关节症状的发作,提示对局部抗原存在持续的免疫应答。
C.感染细小病毒B19、EB病毒、B型肝炎病毒或其他致病菌可引发类似RA的自限性关节炎。
D.发生胃肠道或泌尿生殖器的感染后可出现慢性关节炎(
反应性关节炎)。
有确凿的证据表明许多抗原参与了RA的发病,但同时也有一些相反的结论。造成这种现象的原因很多,包括研究对象在遗传、种族或人种方面的差异,社会经济的差异,疾病持续时间的长短,以及接受治疗的方法不同等,而且,检测抗原的方法也是多样的。下面将对RA出现的主要抗体分别进行介绍。
(6)类风湿因子:针对IgG的Fc段产生的特异性自身抗体是RA一个重要的免疫异常表现。对RA来说,类风湿因子(RF)并不具备特异性,因为在健康人和诸如慢性细菌性感染、器官移植和某些慢性炎性疾病等患者中也可出现。而且,RF出现的频率随年龄的增长而增高。大约80%RA患者的血清中可以检测到RF。尽管有诸多的限制条件,目前仍然将RF作为诊断RA的主要实验室指标。
多年的研究表明,有许多证据支持RF在RA的发病中有着重要的作用,它们是:①RA的严重程度和疾病的活动性与RF的水平相关。血清阳性的RA患者较血清阴性的RA患者出现关节外症状的频率更高(如类风湿结节、血管炎等),而且前者的血沉增快,补体水平升高,侵犯的关节数目增多;②滑膜是RA炎症反应主要发生的部位,它可以局部产生RF;③RF是血清、滑液、滑膜组织和软骨组织中免疫复合物的主要成分;④多克隆IgM RF可以通过经典途径固定和激活补体;⑤向RA患者的关节内注射RF可以促进炎症反应;⑥血清RF阳性的无关节症状者出现RA的危险性明显增加。
尽管有证据表明抗原介导的反应可以作为RF的调节剂,但是启动RF产生的机制尚不清楚。尚无证据显示免疫球蛋白基因是诱导RF产生的遗传危险因素。源自B细胞的肿瘤常可分泌带有限制性Vκ基因片段的RF;而用来形成类风湿关节炎RF的免疫球蛋白V基因片段的所有组成成分并不是惟一的,因为位于免疫球蛋白重链和轻链中的许多不同片段都可作为RF所有组成成分的代表,即RF包含一整套异质性胚系基因(germinal gene)成分。这似乎看来RA滑膜和外周血中产生RF的B细胞是抗原驱动反应的结果,而不是多克隆B细胞刺激的结果。目前尚不清楚遗传因素和外源性因素在促进多克隆B细胞活化过程中的作用。
在动物实验中可以看到,lpr小鼠的fas凋亡基因突变后可以产生高滴度的RF。包括凝集素和超抗原在内的多克隆刺激剂可以诱导RF的产生。如果将B细胞置于成纤维样滑膜细胞和IL-10的条件下进行培养,RF的产生明显增加。体外实验显示,在T细胞的作用下,RF可以发生同型转换和亲和性成熟。另外,RF阳性的B细胞增殖多发生于滑膜组织,因为这里是RF产生的部位。
RA患者的血清中出现RF,说明机体失去了免疫耐受。许多研究者对RF转基因小鼠的B细胞免疫耐受的调节进行了研究,并证实了上述现象。
在疾病的发展过程中,RF有以下一些作用:①含有RF的免疫复合物沉积于多种组织中,有可能通过参与滑膜组织和RA血管炎的炎症反应,激活补体级联反应,参与免疫损伤;②RF在RA中的作用与它正常的生物学功能密切相关,由于RF能够与IgG结合,使得表达RF的B细胞可以捕获由免疫复合物获得的抗原。与抗原特异性B细胞一样,RA中产生RF的B细胞可以作为IgG-抗原复合物的抗原递呈细胞,将免疫复合物含有的抗原递呈给抗原特异性Th细胞,以维持局部免疫应答,并刺激前炎症性细胞因子的产生;③IgG-RF可以进行自我识别,在一定的浓度下,可以形成二聚体和小的多聚体。有实验支持,这些复合物与CD16A(巨噬细胞上低亲和力的Fcγ受体)的结合可能是启动和促进慢性炎症的重要机制;④在对RA患者进行的试验中,将取自患者的RF注入一个关节,而将正常的IgG注入另一个关节,结果前者出现剧烈的炎症反应,后者则未出现。而且动物模型也证实了单独注入针对某一自身抗原的自身抗体可以引起疾病的转移。研究表明,该模型致病性的自身抗体对葡萄糖-6-磷酸异构酶有特异性。葡萄糖-6-磷酸异构酶是糖酵解途径中的一种酶,机体每个细胞都可表达该酶。但尚不清楚具有这种特异性的自身抗体是如何诱导关节炎症的。值得注意的是,这些结论来自对动物关节炎模型的观察。尚无直接证据显示人类RA产生的RF具备上述作用。
(7)RA的其他自身抗体:
①抗热休克蛋白dnaJ抗体:E.coli是热休克蛋白hsp65的成员之一,后者在DNA复制过程中起一定作用。细菌中的热休克蛋白通过分子模拟对启动类风湿关节炎B细胞的免疫应答有重要作用。推测认为,如果外源性抗原的序列与内源性抗原MHC的序列相同,那么可以引起有可能致关节炎的肽类不恰当的递呈,导致其他正常组织发生炎症反应。分子模拟在破坏自身免疫性疾病的B细胞耐受方面有一定作用。已有研究者在免疫球蛋白转基因小鼠模型中证实了模拟自身抗原的外源性抗原可以解除B细胞的外周耐受(peripheral tolerance),并有多个试验证实细菌dnaJ蛋白可能参与了RA的启动。
②抗软骨的自身抗体:已有很多证据支持软骨蛋白和蛋白多糖在RA发病中的作用。在BALB-c小鼠中,Ⅱ型胶原、聚合素、软骨连接蛋白和人软骨gp39都可诱导关节炎的发生。同时也有证据表明这些抗原在RA中可发生免疫反应。
A.Ⅱ型胶原:给大鼠、小鼠和灵长类动物免疫天然的Ⅱ型胶原可引发与RA相似的炎性关节炎。与其他类型的关节炎相比,在RA患者的滑膜中常可检测到抗Ⅱ型胶原抗体。如果在RA的早期发现该抗体,将预示有可能出现较为严重的症状。有实验显示,与对照组相比,口服Ⅱ型胶原的RA患者关节疼痛和肿胀的表现明显减轻。目前认为抗胶原抗体的致病机制可能是通过形成免疫复合物,激活补体从而引发炎症反应。因为在RA病人的血清及关节液中都可检出含有胶原的免疫复合物,而且这些免疫复合物均结合有C1q。不过,抗胶原抗体出现于RA发病之后,所以认为它是继发于关节组织的破坏,同时又参与关节组织的破坏,促进RA病程的发展。
B.人软骨糖蛋白39:在RA,人软骨糖蛋白39(HCgp39)是近来引起研究者关注的候选自身抗原。它是壳多糖酶家族的糖蛋白成员之一。它的功能目前尚未被清楚认识。HCgp39最初是从RA患者的滑液和血液中分离得到的,被认为是关节损伤的生化标志。它在关节的软骨细胞和滑膜细胞表达。用HCgp39免疫BALB-c小鼠可以诱发慢性可复发的关节炎,而对人RA来说,它可诱发血管翳的产生和软骨的降解。用HCgp39预处理的BALB-c小鼠表现出疾病发作的延迟和疾病活动度的减弱,这说明在动物模型中HCgp39可以诱导免疫耐受。而且用它可以成功地缓解处于活动期BALB-c小鼠的病情。这些资料显示了HCgp39作为维持滑膜B细胞反应的自身抗原在RA中的作用。 C.聚合素和软骨连接蛋白:聚合素(aggregation)是含有核心蛋白的软骨蛋白多糖(proteoglycan),它的糖胺聚糖侧链连有硫酸角质素和硫酸软骨素以及以N-连接和O-连接的寡糖。聚合素的结构包括三个球形区(G1、G2和G3)。软骨连接蛋白是一种小的糖蛋白,它起到稳定聚合素与透明质酸的作用。用非糖基化的核心蛋白或G1结构区免疫BALB-c小鼠可出现与RA相似的进行性多关节炎。在一部分RA患者的血清中可以检测到抗聚合素G1结构区的抗体。糖基化的蛋白多糖是诱导小鼠出现关节炎的重要组成成分。从软骨中释放出的蛋白多糖片段在维持RA滑膜异常免疫应答中起重要作用。
③应用于临床检测的自身抗体:
A.抗角蛋白抗体(antikeratin antibody,AKA):用间接免疫荧光法染色大鼠食道中段的角质层可以检测到AKA。AKA呈平滑的板层状。这种组织还可出现其他染色图形,但不仅仅局限于RA患者的血清中,因此必须加以排除。AKA-IgM对RA是非特异性的,而AKA-IgG对RA有高度的特异性。不过,纯化的角蛋白抗体对RA的特异性并不很高,这可能是由于RA特异性抗原是角质层中不同的成分。有50%左右的RA患者可出现AKA,而在正常人有0%~3%。尽管AKA检测的敏感度很低,但是它对RA的特异性达到95%~100%。更重要的是,约有34%的类风湿因子阴性的患者可出现AKA,在这类患者中,AKA具有一定的诊断意义。
B.抗核周因子(antiperinuclear factor,APF):上皮细胞颗粒层的透明角质颗粒中可以检测到核周因子抗原。这种颗粒呈卵圆形,直径0.2~0.3µm,每个细胞可有2~10个。只有合成软角蛋白的颊黏膜和食道黏膜等上皮细胞才表达这种抗原。目前已知这种抗原与profillagrin有关。APF的检测与常规的抗体实验室检测方法不同,因为产生这种抗原的细胞系很少,不太容易找到合适的供者(仅有10%的人其颊黏膜具有APF)。健康者的APF滴度为1∶5,而自身免疫病患者该抗体的滴度是1∶800。APF可以在RA、SLE、系统性硬化和传染性单核细胞增多症等患者的血清中出现。在RA,该抗体检测的敏感性高于AKA,但特异性低于后者。类风湿因子阴性的RA患者出现APF与疾病的严重程度、关节外表现,以及放射学的表现进展有关。
C.抗HnRNP蛋白抗体:约有47%的RA患者血清中存在IgG型抗异质性核RNP(Hn-RNP)核心蛋白A1的抗体。HnRNP复合物与前-mRNA有关,它与小nRNPs、Sm和nPNP不同,后者主要被SLE患者体内的抗体所识别。有趣的是,AKA的活性与抗A1抗体的出现相关,这表明AKA与HnRNP A1抗原有交叉反应。
1/3的RA患者可以检测出抗RA33kD抗体。该抗体在正常人血清中不存在,因此该抗体成为另一个血清学诊断有用的抗体。RA33kD也属于HnRNP核心蛋白,但它有别于A1。
D.抗聚角蛋白微丝蛋白抗体(anti-filaggrin antibody,A
FA):聚角蛋白微丝蛋白产生于哺乳动物上皮细胞分化的终末阶段。它是以原聚角蛋白微丝蛋白(profilaggrin)的前体形式在角质上皮组织中合成的。原聚角蛋白微丝蛋白沉积在上皮细胞的颗粒内,在细胞分化的过程中,经蛋白水解作用,释放出的聚角蛋白微丝蛋白。在这个阶段蛋白脱磷酸,约有20%的精氨酸残基经精氨酸脱亚氨基酶的作用转化为瓜氨酸。30%~40%的聚角蛋白微丝蛋白的氨基酸残基的重复单位变化多样,因此,聚角蛋白微丝蛋白的氨基酸序列存在很大的异质性。这也是A
FA在临床应用中最大的阻碍。
A
FA是与RA相关的IgG型自身抗体,其中包括AKA和APF。A
FA采用免疫印迹法或ELISA进行检测,有文献报道,该抗体的灵敏性和客观性较AKA和ARF的间接免疫荧光试验结果高。过去认为A
FA识别人类上皮组织的聚角蛋白微丝蛋白以及其他与原聚角蛋白微丝蛋白相关的蛋白。20世纪90年代末,在体外通过精氨酸脱亚氨基酶重组人聚角蛋白微丝蛋白得到A
FA蛋白的抗原决定簇,而且2/3来自聚角蛋白微丝蛋白合成多肽的中心部位是瓜氨酸。肽链分别与纯化的A
FA抗体、RA血清反应,只有含瓜氨酸的肽链才能被RA血清和A
FA抗体特异性识别。这些说明,瓜氨酸,是RA血清抗聚角蛋白.微丝蛋白相关抗体识别的主要组成性抗原决定簇成分。因此,人工合成的抗环瓜氨酸多肽抗体(anti-CCP antibody)。有文献报道,在敏感性方面,抗CCP抗体与RF相似,但特异性较后者有明显增高。Kroot等人临床观察认为,抗CCP抗体阳性的RA病人,骨质破坏的程度,较该抗体阴性者严重。由此可见抗CCP抗体对于RA的早期诊断和预后评估有一定的意义。
(8)固有免疫在类风湿关节炎中的作用:固有免疫(innate immunity)指的是对感染因素的非抗原特异性免疫应答,包括抗微生物肽、补体激活途径、甘露糖结合凝集素(mannose binding lectin,MBL)系统、自然杀伤细胞以及细胞因子的释放等在内的效应机制。与此相反,获得性免疫(adaptive immunity)是通过T细胞或B细胞产生抗原特异性的免疫应答,具有分辨自我和非我的功能。固有免疫应答不仅有促进炎症反应的作用,而且还可对获得性免疫有刺激或抑制作用。
研究固有免疫在RA中的作用,前提是某种感染因素直接刺激固有免疫系统,或机体释放可以启动滑膜炎症的非特异性细胞因子,尽管目前尚不知这种感染因素是什么。
有人提出,RA的发病似乎开始于滑膜衬里层细胞。这些细胞产生趋化因子,使得单核细胞和淋巴细胞进入关节内。如果单核细胞或淋巴细胞识别出关节内的某一种(或几种)抗原,那么淋巴细胞就会被保留下来,接着发生炎症反应。这个有“毒性”的环境可以改变T细胞表型。这个假设不需要某种特异性的致病因素,任何一种进入关节的病原体都可激发固有免疫应答。
根据对动物早期炎症性关节炎发病机制的研究,有人认为在RA也可出现类似的表现。固有免疫作为原始的推动力有可能在RA早期阶段吸引抗原特异性免疫应答,并有可能推动这一过程的进程。组织学的研究显示,固有免疫系统在启动RA滑膜炎症中的作用包括:滑膜中非特异性炎症可以刺激巨噬细胞释放细胞因子,导致树突状细胞分化并形成有效的抗原递呈细胞;滑膜中成熟的树突状细胞可以将抗原递呈给记忆性T细胞,诱导产生Th1或Th2反应;巨噬细胞可以吞噬细菌的片段,包括从机体黏膜表面进入关节的具有免疫刺激性的DNA;细菌产物刺激巨噬细胞分泌的局部细胞因子并再次激活树突状细胞、B细胞和自然杀伤细胞;关节内活化的补体系统增强局部的炎症反应和B细胞反应。
在RA滑膜中可以检测到固有免疫系统的主要细胞和分子,它们有可能通过非特异性抗原机制参与炎症的启动。但是,诸如补体抑制剂、MBL系统、成熟的树突状细胞、NK细胞的抑制性受体、抗炎性细胞因子以及细胞因子的拮抗剂等固有免疫系统的自然调节机制不足以阻止RA滑膜炎的发展。其中,固有免疫系统调节机制存在的缺陷有可能是遗传因素决定的,也可能受环境因素的影响。这些异常的调节机制在病人中表现为多种形式。不过,目前尚不清楚在RA中固有免疫是起非特异性的辅助作用,还是作为致病的主要形式存在。
4.骨与软骨的破坏 RA与其他炎症性关节病不同之处在于其滑膜有过度增生的倾向,并可对与滑膜接触的局部软骨与骨,产生侵蚀作用。多种机制参与了这一过程(表6)。软骨与骨并不是组织遭到破坏的惟一目标,软骨细胞和破骨细胞也参与了组织细胞外间质的丢失过程,而且RA关节破坏的目标还包括韧带和肌腱。
在生理条件下,人体的软骨与骨的合成和降解处在一种动态的平衡中,而这种平衡在RA被多种因素破坏,造成结缔组织的持续降解,以致出现软骨与骨的进行性和不可逆性破坏。其中参与的因素包括:①诸如IL-1等细胞因子对关节完整性的破坏有重要作用;②血管生成素以及能够促进血管生成的其他因子,它们不但能增强炎性细胞侵蚀关节组织的能力,还可向炎症性细胞和增生细胞提供充足的养料;③趋化因子可将嗜中性粒细胞带入关节腔内,这些趋化因子包括C5a、白三烯B4和血小板活化因子,在关节腔内嗜中性粒细胞释放蛋白酶和趋化分子;④纤溶酶,是由纤溶酶原激活物作用于纤溶酶而形成的,可以使蛋白酶的释放起到放大的作用;⑤滑膜组织产生的中性蛋白酶包括胶原酶和间质溶素,主要参与对软骨与骨的侵蚀;⑥纤维蛋白覆于滑膜和软骨上,凝血的级联反应可进一步促进组织的损伤。尽管许多介质存在天然的抑制剂,但它们都不足以减弱RA的炎症反应。
(1)软骨破坏的机制:关节软骨是由大量的间质和少量的软骨细胞组成的。其中,胶原纤维、蛋白多糖、水等组成软骨间质。软骨细胞可合成并分泌胶原蛋白、蛋白多糖以及其他作用于间质的蛋白。RA软骨的破坏主要是指细胞间质的降解,这一过程实际上是间质被水解蛋白酶消化的过程。
RA软骨的破坏是酶和力学作用的过程。在IL-1、肿瘤坏死因子-α等细胞因子的刺激下,滑膜内细胞释放各种降解软骨间质的酶,它们或以游离的形式,或以与离子结合的形式造成关节的破坏。在滑膜炎早期,在IL-l等作用下,多种蛋白酶使软骨细胞的蛋白多糖逐步被消化,导致软骨的力学作用减弱。当蛋白多糖完全从软骨中消失,软骨即失去对外界负重造成变形的恢复能力。随着胶原酶和间质溶素对软骨的作用,最终使其失去了功能的完整性。另外,有证据表明,软骨细胞也可产生金属蛋白酶。研究显示,RA软骨间质溶素和胶原酶mRNA水平明显增加。因此,软骨的破坏是在多方面机制的作用下完成的,不仅有富含蛋白酶的滑液的作用,侵蚀性血管翳的作用,而且还有软骨细胞自身的破坏作用。
(2)局部骨侵蚀的机制:RA的放射学的改变包括近关节处出现骨质减少、软骨下骨的局灶性骨侵蚀和血管翳侵袭关节边缘。已有多项研究表明,有关局部的骨侵蚀随着疾病的进展而加重,一般来说与疾病的严重程度相关。
①RA局部骨侵蚀的细胞机制:许多证据显示,在正常生理状态下破骨细胞主要起骨吸收作用。它来自于单核细胞/巨噬细胞的前体,通过表达独特的整合素、基质金属蛋白酶和组织蛋白酶K和抗酒石酸磷酸酶完成骨吸收的作用。在RA,抗酒石酸磷酸酶(TRAP)是一种破骨细胞的标记物,表达于破骨细胞表面。这说明破骨细胞可能在RA骨侵蚀方面有一定作用。另外,破骨细胞与其前体的最大不同是前者表达降钙素受体,该受体可与多肽激素降钙素结合,使得破骨细胞骨吸收的作用受到抑制。
矿化的骨细胞外间质对蛋白酶的攻击有保护作用。局部骨侵蚀的第一步是招募并分化表达破骨细胞表型的细胞。在骨骼受侵蚀的部位具有典型的多核巨细胞,它可表达所有成熟的破骨细胞基因,这些基因包括酸性磷酸酶、组织蛋白酶K和降钙素受体。邻近血管翳含有大量的巨噬细胞,它们产生IL-1、肿瘤坏死因子-α,并与来源于T细胞的细胞因子IL-17等的炎性介质,将多核巨细胞分化成破骨细胞。根据对动物模型的研究发现,可溶性破骨细胞分化因子的受体和osteoprotegerin有阻止骨受到侵蚀的作用。
生理性的骨重塑主要是重吸收的骨与新形成的骨两者之间的数量保持一种动态平衡,而RA患者这种平衡被破坏。确定是否由破骨细胞或其他类型的细胞造成局部骨吸收导致出现骨侵蚀,对于理解RA局部骨丢失的作用机制是一个关键。
②调节破骨细胞分化和活化的因子:近来,越来越多的证据表明,细胞因子参与调控破骨细胞的分化和活化。包括可以直接作用于破骨细胞前体诱导其增生和分化的因子,诸如M-CSF、IL-6、IL-11、IL-1α或IL-1β和肿瘤坏死因子-α等。还有许多因子间接地参与了破骨细胞这一过程,包括甲状旁腺激素、与甲状旁腺激素相关的多肽、1,25(OH)2维生素D3、前列腺素E2、IL-11、雌激素和糖皮质激素等。令人感兴趣的是,IL-1α或IL-1β可以直接作用于破骨细胞,而肿瘤坏死因子 α通过作用于破骨细胞的前体间接地起到增强破骨细胞活性的作用。
最近发现一种被命名为破骨细胞分化因子(osteoclast differentiation factor,ODF)也有称之为osteoprotegerin配体(OPGL)或与肿瘤坏死因子相关的诱导激活细胞因子,它是分化破骨细胞有效的调节剂,是由滑膜中成纤维样细胞分泌的。该因子是肿瘤坏死因子配体家族的膜结合成员。ODF主要对破骨细胞的成熟过程起调控作用。成骨细胞和活化的T细胞也可以产生ODF,其中T细胞可能对RA中破骨细胞和成骨细胞功能的平衡起到一定作用。研究显示,许多增强破骨细胞形成或其活性的因子都需要通过下调ODF(或OPGL)的表达才能产生介导对破骨细胞或衬里层细胞的作用。
还有一组因子将ODF作为NF-κB配体的受体激动剂(RANKL),成为促进T细胞的生长和树突状细胞功能的因子。该因子又被称作RANKL/ODF。研究发现,ODF的信号受体就是NF-κB的受体激动剂(RA2NK),它在多种细胞表面表达,包括破骨细胞和破骨前体细胞、某些B细胞和T细胞以及树突状细胞。ODF与RANK的相互作用可使前体细胞分化为破骨细胞,这些因子的过度表达可造成骨的再吸收。
此外,还检测到RANKL/ODF的可溶性“decoy”受体,被称为osteoprotegerin(OPG)。OPG相当于破骨细胞形成抑制因子。在结构上它与RANK不同,但是它可结合破骨细胞分化因子,阻止后者对破骨细胞的分化或活化。
③参与RA局部骨侵蚀的因子:RA滑膜组织产生大量与调节生理骨重塑相关的因子,其中包括IL-1a或IL-1β、IL-6、IL-11、M-CSF和肿瘤坏死因子-α。对RA动物模型的研究显示,IL-1和肿瘤坏死因子-α在炎性关节炎局部骨侵蚀的发病中有非常重要的作用。例如,在胶原性关节炎的动物模型中,给予能够中和IL-1的抗体即可阻止骨和软骨的破坏。此外,有人发现虽然阻断肿瘤坏死因子-α可以减轻RA的炎症,但是只有阻断IL-1才能防止骨与软骨的丢失。不过,对于RA患者在临床上应用IL-1和肿瘤坏死因子-α抑制剂可减轻关节的炎症表现,并可推迟骨侵蚀的进展。
最近,一研究小组对RANKL/ODF在RA骨重吸收机制中的作用进行了描述。应用原位杂交和RT-PCR技术,他们发现取自RA滑膜组织培养的成纤维细胞和活化的CD4 淋巴细胞可以表达ODF mRNA;同样,取刚分离的,RA滑膜组织的CD4 和CD8 淋巴细胞也表达ODF mRNA。应用免疫荧光可直接证明RA滑膜中有RANKL/ODF蛋白的存在。Kong等人用佐剂性关节炎的动物模型研究表明,ODF、在破骨细胞介导的骨重吸收中有一定作用,例如,给予刚发病的动物一定的OPG,可以看到骨皮质和骨小梁的骨丢失被完全抑制。
(3)各种类型的细胞在RA关节破坏中的作用:在RA早期,由于滑膜衬里层细胞数量的增多和细胞形态的肥大造成滑膜增厚。促炎症性细胞因子IL-1和肿瘤坏死因子-α刺激黏附分子在内皮细胞的表达,并增加招募嗜中性粒细胞进入关节腔。嗜中性粒细胞可释放蛋白酶,主要降解软骨表层的蛋白多糖。当蛋白多糖全部消化后,免疫复合物便进入胶原的表层,并暴露出软骨细胞。在IL-1和肿瘤坏死因子-α的刺激下,或在存在活化的CD4 T细胞情况下,软骨细胞和滑膜成纤维细胞可释放MMPs。随着病情的进展,滑膜组织逐渐转变为炎性组织,其中一部分有新的血管生成,即形成血管翳。这种组织具有侵蚀和破坏邻近的软骨和骨的功能。
5.类风湿关节炎发病机制的模式 随着越来越多的细胞因子被发现,以及对TCR和巨噬细胞/成纤维细胞功能研究的深入,使得研究者重新修订传统的RA发病机制的模式。近来提出一范例试图解释在巨噬细胞/成纤维细胞高度活化的情况下,RA滑膜组织出现的T细胞应答反应。目前一致认为,RA的起始阶段有可能是由T细胞介导的一抗原特异性的过程。致关节炎抗原尚未发现,有可能是反转录病毒、某种细菌的产物或其他生物体,如衣原体、分枝杆菌、螺旋体等。对于RA易感者而言,出现早期T细胞的应答,导致细胞因子的分泌,随后招募包括嗜中性粒细胞、巨噬细胞、B细胞和记忆性T细胞在内的多种炎性细胞,它们具有广泛的抗原特异性。当疾病确立后,逐渐分化为3种RA基本模式。不过,重要的是,必须清楚地认识到这3种模式只是用来解释慢性滑膜炎发展的持续阶段,而非疾病的起始阶段。同时,还应该了解这3种模式并不是各自孤立的,而是可以相互作用的(图3)。
(1)T细胞介导的免疫应答:如果滑膜组织中持续存在某种致关节炎抗的免疫应答。已有许多实验结果支持这一论点。例如,莱姆病的关节损害与RA十分相似,而莱姆病的致病抗原就是螺旋体抗原。HLA-DR的表面密度在滑膜衬里层细胞和巨噬细胞很高,这说明存在活跃的抗原递呈活动。此外,来自滑液和衬里层下组织的T细胞常表达细胞表面活化的标记物,如MHCⅡ抗原和转铁蛋白受体。位于“过渡区(transitional areas)”的淋巴细胞与富含HLA-DR的辅助细胞密切相关。这些活化细胞的产物有可能诱导MHCⅡ抗原的表达,促使滑膜衬里层细胞的增生,并支持B细胞的生长与分化。诸如胸导管引流、全身淋巴放疗和环孢素A等针对T细胞的特异性治疗对RA病情的改善有一定作用,这一事实也支持T细胞介导的免疫应答在RA中有重要作用。
T细胞介导的免疫应答产生RA滑膜炎这一观点从理论上可以解释RA的许多特征,包括:①T淋巴细胞的聚集;②滑膜衬里层细胞过度增生;③B细胞过度活跃,局部产生自身抗体。
不过,目前有一些现象尚不能用这一模式解释:①关节内产生的可溶性介质来源于非T细胞;②现有手段检测到T淋巴细胞产生的细胞因子的数量非常少;③来自T细胞介导的因子在人类其他T细胞介导的疾病中也可检测出,如胸膜结核、皮肤的迟发型超敏反应或过敏原诱发的哮喘等。这些问题的出现使得研究者提出了RA发病的其他假设模式。
(2)自身反应性T细胞:RA的慢性关节损伤可能是对抗原应答的结果,这与疾病的起始阶段不同。在其他自身免疫性疾病中也曾提出过相似的发病机制,例如,
自身免疫性甲状腺炎即是对某种推测病毒的侵袭产生适当的免疫应答,导致局部分泌IFN-γ,后者诱导甲状腺细胞表达HLA-DR,使之成为免疫攻击的对象或作为抗原递呈细胞。携有HLA-DR的刺激细胞与自身T淋巴细胞之间的反应被称作自身混合性淋巴细胞反应(autologous mixed leukocyte reaction,AMLR)。RA患者的滑膜可出现局部的AMLR,主要有以下依据:①富含细胞因子的RA滑膜与AMLR中的情况非常相似,即诸如IL-2和IFN-γ等来自T细胞的细胞因子数量非常少;②RA关节液中检测到的细胞毒性T淋巴细胞与AMLR产生的NK样细胞具有相似性;③关节腔和关节滑膜中含有多种潜在的刺激细胞,它们与应答细胞的位置非常接近。其中应答细胞包括A型滑膜细胞和树突状细胞,后者是AMLR最有效的刺激物。
除了MHCⅡ抗原外,慢性滑膜炎中的滑膜T细胞可以直接针对其他自身抗原产生应答,并被释放至富含T细胞的环境中。针对Ⅱ型胶原的免疫应答就是其中的一个例子。此外,也可通过分子模拟的方式使自身反应性T细胞受到刺激,例如,热休克蛋白、蛋白多糖和EB病毒就是通过这种方式产生免疫应答的。
(3)旁分泌/自分泌模式:前面提及的RA持续阶段的两种发病机制的模式主要围绕着T淋巴细胞。在这些模式中,T细胞的产物分布于整个组织中,直接刺激滑膜衬里层下的巨噬细胞和滑膜细胞,诱导黏附因子表达于后毛细血管高内皮细胞静脉,并通过B细胞的增生与分化刺激局部免疫球蛋白的产生。不过,正如前所述,研究发现关节腔内活化的T细胞的产物不仅数量少,而且所起的作用也不大(表7)。
与之相反,滑膜内巨噬样细胞和成纤维样细胞分泌的细胞因子,如IL-1、肿瘤坏死因子-α、IL-6、GM-CSF、M-CSF、TGFβ、前列腺素、补体蛋白、TIMP、胶原酶等,在滑膜组织和滑液中的含量十分丰富。根据超微结构分析和细胞表面HLA-DR的表达,显示这些细胞具有活化的表型。这些表明,RA的慢性滑膜炎是在T细胞作用下产生的这一传统观点应该有所改变。也就是说,关节衬里层邻近的巨噬细胞和滑膜成纤维样细胞以旁分泌或自分泌的形式产生大量的细胞因子,维持并促进滑膜炎症的发生与发展。在关节腔内已识别出多种参与这一过程的细胞因子,并能解释滑膜衬里层细胞的增生、HLA-DR的诱导和滑膜新生血管的形成。
图4是存在于滑膜细胞间复杂的细胞因子网络示意图,涉及巨噬细胞和成纤维细胞,由于T细胞分泌的细胞因子难以检测,故其细胞因子是否参与疾病的过程尚不清楚。
IL-1和肿瘤坏死因子-α都是由滑膜巨噬样细胞分泌,它们可以刺激成纤维样细胞的增生,增加IL-6、GM-CSF和诸如间质溶素和胶原酶等效应分子的分泌。GM-CSF是由滑膜巨噬样细胞以及在IL-1β或肿瘤坏死因子-α刺激下的成纤维样滑膜细胞产生的,它是IL-1、肿瘤坏死因子-α和IL-8产生的诱导剂。特别是在肿瘤坏死因子-α的协同下,GM-CSF还可以增加巨噬细胞和单核细胞表面HLA-DR的表达。成纤维样滑膜细胞具有自分泌反馈环,可以通过分泌成纤维细胞生长因子(FGF)作用于自身的调节。巨噬细胞和成纤维细胞产生的局部细胞因子还可作用于T细胞,并能适度调节T细胞的活性。B细胞的活化以及RF的产生有可能是非T细胞作用机制的结果。因为转化表型依赖于FGF和PDGF等细胞因子以自分泌形式的刺激,所以说具有转化特性的滑膜细胞也符合旁分泌/自分泌的特点。据推测,这一模式还有一个特点,即细胞因子以非抗原特异的方式吸引T细胞进入关节滑膜。
细胞因子的抑制剂在自分泌/旁分泌模式中也发挥着一定作用,因为负反馈环可能是一种重要的调控滑膜炎症反应的正常内环境稳态机制。不过,这些抑制剂并不能有效地阻止,促炎症性细胞因子的作用。例如,从理论上讲,IL-1Ra能够对RA的发展有一定的阻碍作用,但事实上,尽管关节内有大量的IL-1Ra,滑膜炎症仍持续进展。
(4)T细胞-巨噬细胞-成纤维细胞轴:上述3种有关RA的发病机制模式实际上包括一系列的基本原理与理论。目前认为,RA滑膜炎症的持续阶段是上述三种模式共同完成的,即是T细胞、巨噬细胞和成纤维细胞相互作用的结果。
我们研究疾病发病机制的目的是为了能够采取更积极主动、更全面的治疗措施。因为RA涉及的这些细胞相互之间的关系错综复杂,所以针对其中任何一种模式的治疗都不可能取得十分满意的疗效。尽管在临床上应用针对T细胞特异性的治疗取得了一些成绩,但是仍然有一部分患者对治疗的反应和疾病的改善程度相对较差。例如,环孢素A是一种主要针对T细胞的治疗药物,临床上只有一小部分患者可以达到50%的改善。也许用于早期RA的治疗会有一定的作用,因为在RA的早期可以出现T细胞介导的损伤,此时使用针对T细胞的治疗或许可以收到更好的效果。
6.病理 类风湿关节炎的病变主要发生在关节腔,有些病人伴有关节外表现。其病理特点是:①炎症细胞浸润,甚至淋巴滤泡形成;②血管炎;③类风湿性肉芽肿形成。
(1)正常关节组织:滑膜是衬在关节囊内面的一层组织,它并不覆盖关节软骨,其表面被A细胞和B细胞各一层所覆盖,据认为A细胞是由个体发育初期固定在该处的巨噬细胞衍变而来,其下面是一层由成纤维细胞衍变来的B细胞。B细胞下面有丰富的毛细血管和细静脉,它们的通透性很高。再下面是以脂肪为主的结缔组织。A细胞有很小的细胞突起,含有丰富的溶酶体,内噬性作用很强,能够清除腔内衰老组织。B细胞表面有丰富的圆形或椭圆形小胞体,能产生胶原、纤维粘连蛋白、层粘连蛋白和透明质酸等基质,起润滑和缓冲作用。同时也具有大量基质合成酶和基质分解酶。血管供给能量,兼有供排水功能。
关节软骨附着于软骨下骨的表面。软骨由软骨细胞和软骨基质构成,软骨细胞合成及分泌基质。基质主要由Ⅱ型胶原、蛋白多糖和水组成。关节软骨无血管和淋巴,它们是通过滑膜液摄取营养的。
(2)滑膜炎症反应:
①衬里细胞层增厚:类风湿关节炎的滑膜衬里细胞从正常的1~2层增厚到8~10层。两类细胞数量均增加,但以A型细胞增加为主。增生的A、B细胞均被活化,高度表达激活抗原。
②新生血管和炎性细胞浸润:类风湿关节炎滑膜的微血管数量显著增加,新生的血管主要为毛细血管及具有高柱状内皮细胞的毛细血管后微静脉,后者在滑膜深处。这些高柱状内皮细胞高度表达多种细胞黏附分子和细胞因子。大量淋巴细胞聚集在血管周围,其中以CD4 T细胞为主,少量CD8 T细胞,形成滤泡样结构。可见少量B细胞在滤泡中心,但大量浆细胞散布在淋巴滤泡周边或之间。巨噬细胞分布在整个滑膜。少量树突状细胞散在于淋巴滤泡中和衬里细胞层。类风湿关节炎滑膜内各类细胞均表达MHCⅡ类分子,其表达的水平显著高于正常人的滑膜。
③血管翳的形成:由于滑膜衬里细胞增厚、新生血管、大量炎症细胞浸润、淋巴滤泡形成,使滑膜发生绒毛样增生,增生的滑膜形成血管翳突入关节腔内。
(3)软骨和骨的破坏:类风湿关节炎关节软骨的破坏开始于滑膜与软骨的交接处。此处滑膜增厚,血管、细胞成分显著增多,形成血管翳并自关节软骨边缘处逐渐向软骨面伸延,构成血管翳/软骨结合。血管翳中增生的A、B型细胞及浸润的炎症细胞分泌蛋白酶(主要是基质金属蛋白酶)、细胞因子(IL-1和肿瘤坏死因子-α等)和其他炎性介质,破坏相邻的软骨,使软骨细胞分泌基质减少,胶原和蛋白多糖被基质金属蛋白酶破坏,破骨细胞被激活,最终导致关节软骨和骨的破坏。
(4)关节腔积液:正常关节腔内有少许滑膜液,膝关节滑液不多于3.5ml,呈草黄色,清亮透明,含有少量白细胞,起润滑关节作用。类风湿关节炎病人关节腔可出现大量积液,尤其在急性期。积液中含有大量炎症细胞,主要为中性粒细胞,还可见到大量T细胞,少量的单核/巨噬细胞、树突状细胞和B细胞。可测到多种细胞因子及可溶性受体(图5)。
(1)晨僵:病变的关节在夜间静息后出现较长时间(至少1h)的僵硬,如胶黏着样的感觉,出现在95%以上的患者。晨僵持续时间和关节炎症的程度成正比,它常被作为观察本病活动指标之一,只是主观性很强,其他病因的关节炎也可出现晨僵,但不如本病明显。
(2)痛与压痛:关节痛往往是最早的症状,最常出现的部位为腕、掌指关节、近端指间关节,其次是趾、膝、踝、肘、肩等关节。多呈对称性、持续性,可时轻时重。疼痛的关节往往伴有压痛。受累关节的皮肤出现褐色色素沉着。
(3)关节肿:多因关节腔内积液或关节周围软组织炎症引起。病程较长者可因滑膜慢性炎症后的肥厚而引起肿胀。凡受累的关节均可肿,常见的部位为腕、掌指关节、近端指间关节、膝关节等,亦多呈对称性。
(4)关节畸形:多见于较晚期患者。因滑膜炎的绒毛破坏了软骨和软骨下的骨质结构造成关节纤维性或骨性强直,又因关节周围的肌腱、韧带受损使关节不能保持在正常位,可导致手指关节的半脱位如尺侧偏斜、屈曲畸形、天鹅颈样畸形等。关节周围肌肉的萎缩、痉挛则使畸形更为加重。
(6)关节功能障碍:关节肿痛和结构破坏都引起关节的活动障碍。美国风湿病学院将因本病影响了生活的程度分为4级:Ⅰ级:能照常进行日常生活和各项工作。Ⅱ级:可进行一般的日常生活和某种职业工作,但对参与其他项目活动受限。Ⅲ级:可进行一般的日常生活,但参与某种职业工作或其他项目活动受限。Ⅳ级:日常生活的自理和参与工作的能力均受限。
(1)类风湿结节:是本病较特异的皮肤表现,出现在20%~30%的患者,多位于关节隆突部及受压部位的皮下,如前臂伸面、肘鹰嘴突附近及枕、跟腱等处。其大小不一,结节直径由数毫米至数厘米、质硬、无压痛、对称性分布。它的存在表示本病在活动期。
①肺间质病变:是最常见的肺病变。见于约30%的患者,有时虽有肺功能和肺X线片的异常,但临床常无症状,早期诊断有赖于高分辨CT。部分患者出现气短和肺功能不全,出现慢性纤维性肺泡炎则预后较差。
RA的关节外表现,往往见于血清类风湿因子滴度高的病人。中心小血管的类风湿血管炎可以引起毛细血管扩张症、皮肤溃疡、神经病变、指(趾)坏疽,以及各种脏器合并症如肠系膜血管梗死、心、肺病变等。



 流行病学
流行病学
 病因
病因



 发病机制
发病机制









 临床表现
临床表现
 并发症
并发症
 实验室检查
实验室检查
 其他辅助检查
其他辅助检查
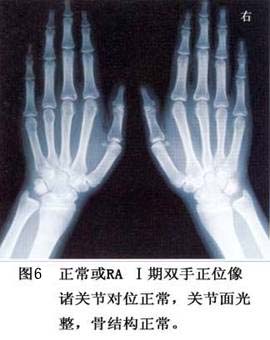









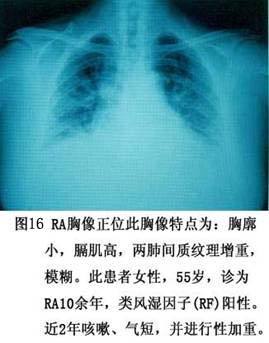


 诊断
诊断
 鉴别诊断
鉴别诊断
 治疗
治疗
 预后
预后
 预防
预防